点击数:202026-03-02 09:49:21 来源: 四川大学 制革清洁技术国家工程研究中心
现代饮食模式中过量的游离糖摄入大幅增加龋病发病风险。当前龋病预防手段忽略了饮食中游离糖的关键致病作用,并对致龋生物膜的抑制效果有限。葡萄糖氧化酶(glucose oxidase, GOx)是解决饮食糖问题的理想候选者,但其在口腔微环境中不稳定、难以维持催化活性。将蛋白质包封在纳米载体中是保护和稳定蛋白质功能的有效策略,但现有的纳米载体仍面临诸多挑战,如酸性环境下稳定性较差、强共价交联损害蛋白质生物活性等。
四川大学制革清洁技术国家工程实验室郭俊凌教授团队长期致力于植物多酚(单宁)的基础科学和前沿应用研究,自2014年构建了由18种金属离子构建的金属多酚网络材料平台(Metal–Phenolic Networks,MPN)以来,团队深入研究了多酚独特的界面相互作用,发展了植物多酚高值转化体系(Science, 2018; Nat. Nanotechnol., 2016, 2025; Nat. Commun., 2022; Sci. Adv., 2021; Cell Biomater., 2025; Matter, 2023, 2025; Angew. Chem. Int. Ed., 2014, 2019, 2023, 2024, 2025; Chem. Soc. Rev., 2022; Chem. Sci., 2025, 2025, 2026; Adv. Mater., 2013, 2020, 2023, 2026等)。
华西口腔医院国家口腔疾病临床医学研究中心/口腔疾病国家重点实验室赵志河教授、方婕副教授联合郭俊凌教授团队创新性提出一种生物质、不含金属的酶–多酚超分子框架材料,构建了一种“牙齿纳米盔甲(Tooth nanoarmor)”,其可粘附于牙釉质表面,长效消耗口腔微环境中的糖从而抑制致龋生物膜的形成。该研究巧妙利用鞣花酸(Ellagic Acid,EA)中心对称的儿茶酚基团与GOx氨基酸残基之间的多重分子相互作用,在生理条件下实现了材料的自组装,有效解决了传统级联纳米酶系统普遍存在的安全性及临床转化障碍,长效调控口腔致龋微环境并抑制致龋生物膜形成,实现龋病预防。该研究成果近日发表于国际顶级期刊Nano Letters。该论文的通讯作者为四川大学郭俊凌教授、赵志河教授及方婕副教授。第一作者为四川大学华西口腔医院张博助理研究员及四川大学制革清洁技术国家工程实验室2021级谢秋萍博士。
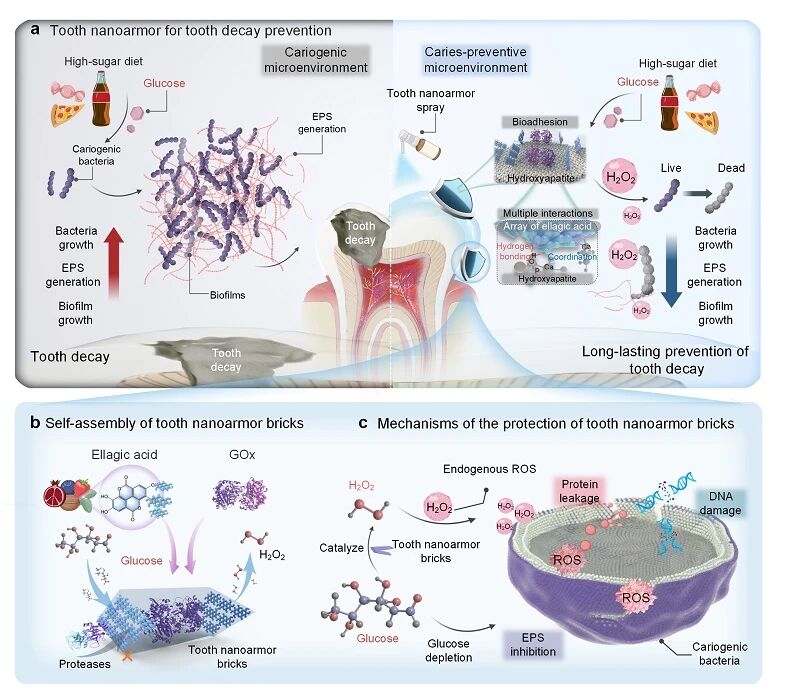
图1. 自组装“牙齿纳米盔甲”长效预防龋病示意图
如图1所示,该团队提出的“牙齿纳米盔甲”由EA与GOx自组装形成,其中EA中心对称的儿茶酚基团与GOx氨基酸残基之间通过氢键和π–π堆积等多种非共价相互作用进行自组装,同时EA的多酚框架通过多种非共价相互作用辅助“牙齿纳米盔甲”粘附于牙釉质表面,位于多酚框架中的GOx可长效消耗口腔微环境中的糖,从而抑制致龋生物膜的形成、预防龋病发生。
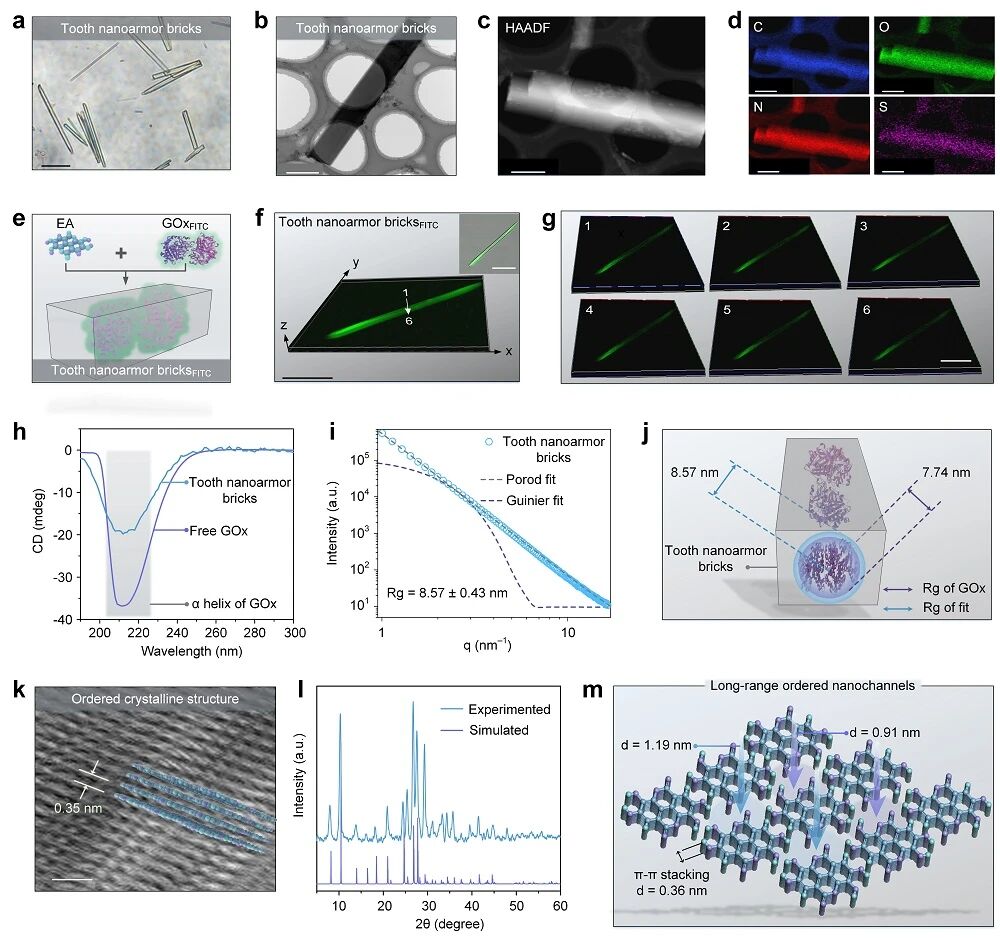
图2. “牙齿纳米盔甲”构建单元材料学表征
光学显微/透射电镜及元素EDS分析证实“牙齿纳米盔甲”构建单元呈现规则棒状结构,且C/O/N/S元素均匀分布(图2a-d)。利用FITC标记的GOx进行自组装后,激光共聚焦z轴切片显示GOx在框架内均一分布(图2e-g)。圆二色谱显示“牙齿纳米盔甲”构建单元保留211 nm特征,表明GOx的α螺旋结构未被破坏(图2h)。小角X射线散射拟合得到介孔尺度可容纳单个GOx(图2i-j)。高分辨透射电子显微镜观察到EA分子π–π堆积(~0.35 nm)(图2k),粉末X射线衍射实验与模拟吻合并揭示有序纳米通道结构(图2l、2m)。
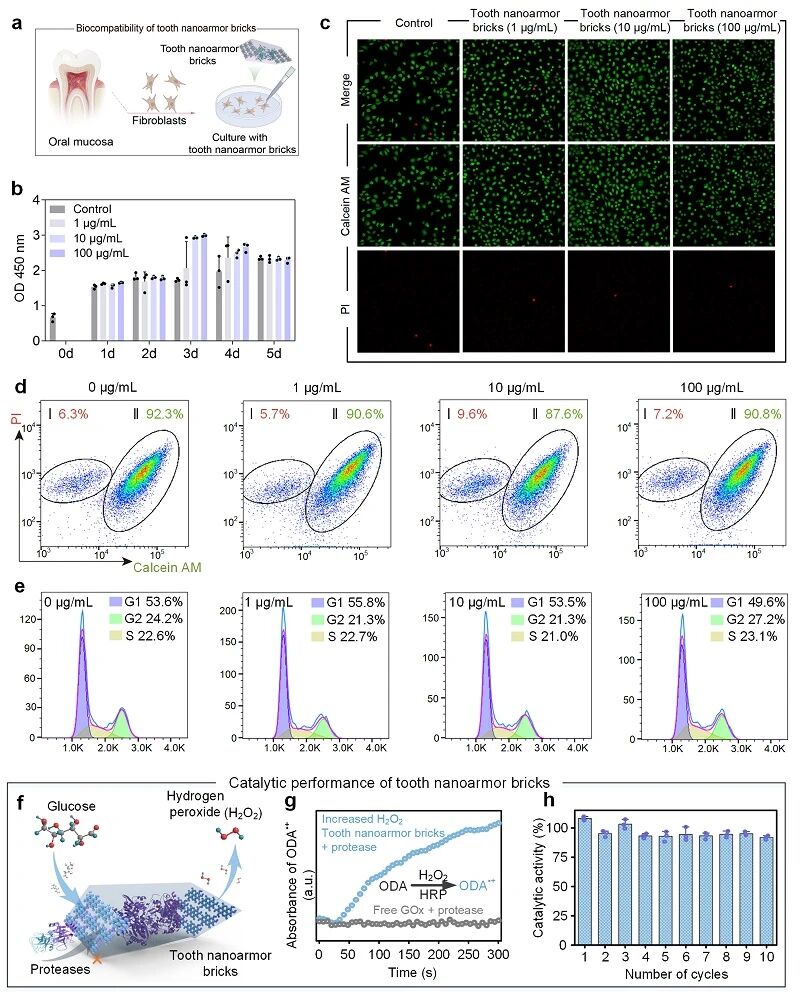
图3. “牙齿纳米盔甲”构建单元生物相容性及催化稳定性
研究团队接下来探索“牙齿纳米盔甲”构建单元生物相容性及催化稳定性,CCK-8与Live/Dead染色未见明显细胞毒性(图3a–c),流式定量显示细胞存活率与对照组想近(图3d)。多酚框架纳米通道允许葡萄糖进入同时阻隔蛋白酶,从而保护GOx催化活性(图3f)。实验显示,在蛋白酶K存在下,游离GOx失活,而“牙齿纳米盔甲”构建单元仍维持催化活性(图3g),循环反应10次仍保留>90%活性,体现高抗降解与可重复催化能力(图3h)。
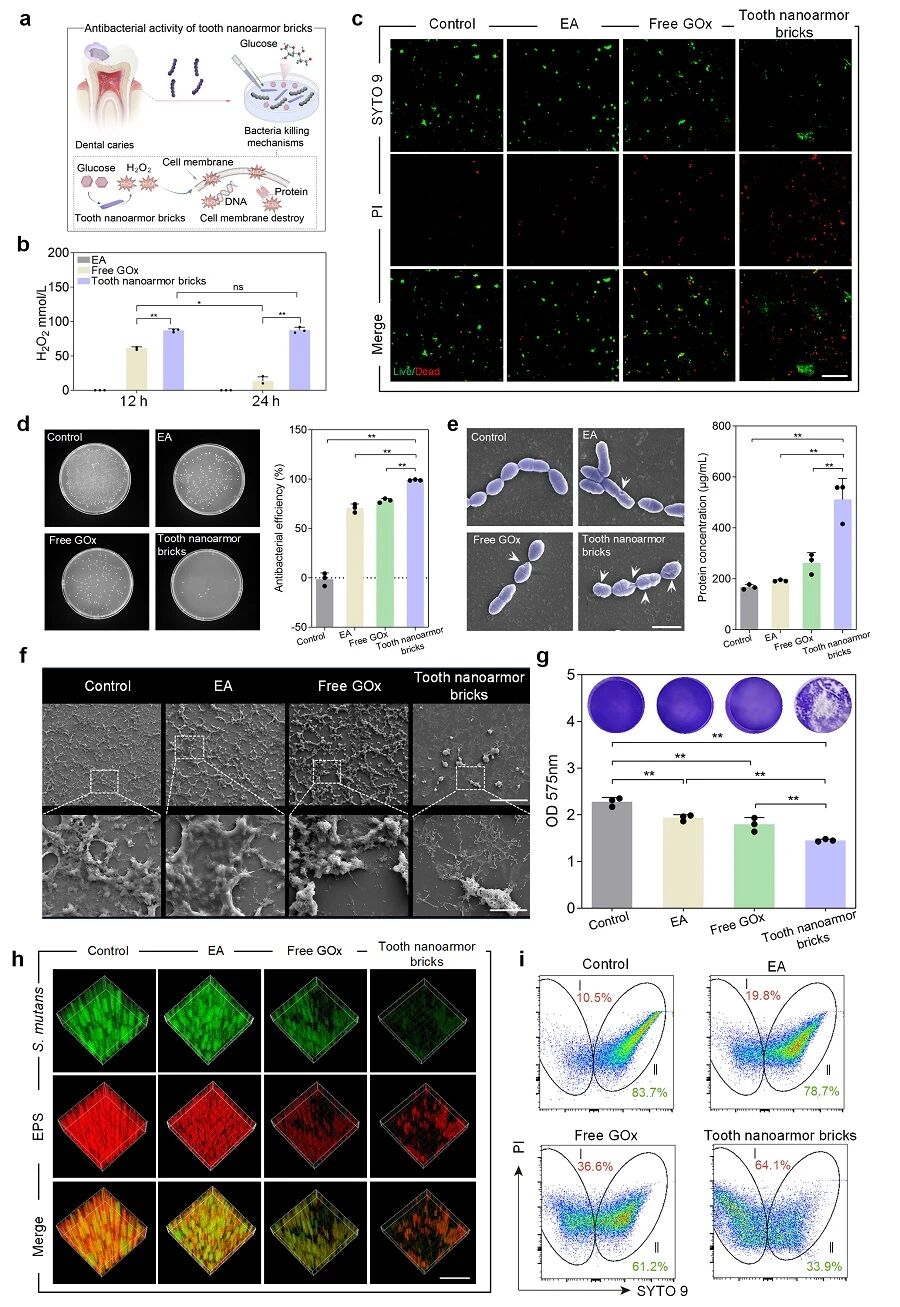
图4. “牙齿纳米盔甲”构建单元抗菌抗生物膜能力
“牙齿纳米盔甲”构建单元得益于其稳定的催化能力,进而展现出良好抗菌抗生物膜能力。实验表明,在含葡萄糖的变异链球菌(S. mutans)培养体系中,“牙齿纳米盔甲”构建单元可持续产生H2O2,优于游离GOx(图4a–b),其对浮游菌具有良好抗菌效应(图4c,d);扫描电镜见细菌皱缩与内容物泄漏,并伴随培养上清蛋白外泄升高(图4e)。在生物膜形成实验中,扫描电镜及结晶紫定量显示生物膜形成被“牙齿纳米盔甲”构建单元抑制(图4f–g);激光共聚焦三维重建显示“牙齿纳米盔甲”构建单元组活菌聚集与胞外多糖生成同步下降(图4h),且流式定量生物膜中活菌比例最低(约33.9%,图4i)。
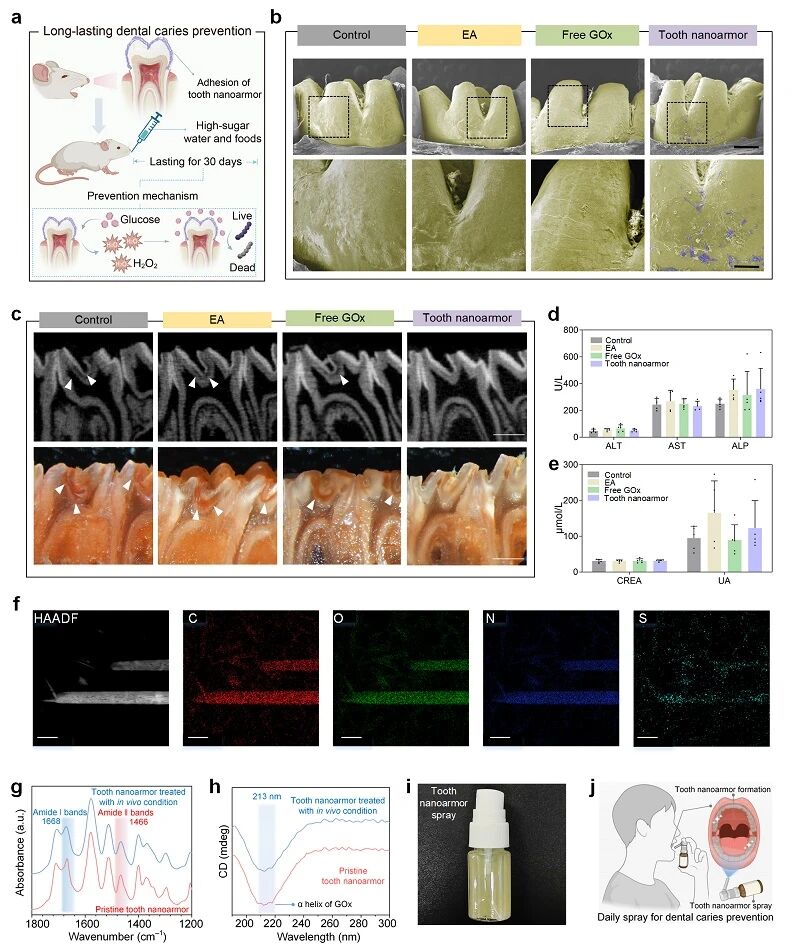
图5. “牙齿纳米盔甲”体内龋病预防能力
研究团队进而采用大鼠30天致龋模型进行体内实验,“牙齿纳米盔甲”构建单元使用后在牙齿表面形成“牙齿纳米盔甲”,扫描电镜显示“牙齿纳米盔甲”处理组牙釉质表面可见棒状材料附着,且釉质表面更平、脱矿凹坑减少(图5a–b)。micro-CT显示,与对照组相比,“牙齿纳米盔甲”处理组龋病Keyes评分在釉质及牙本质损伤(E、Ds、Dm、Dx)评分上显著降低,牙本质密度升高(图5c)。体内生物安全性方面,血生化与组织学染色未见明显异常(图5d–e)。透射电镜、傅里叶变换红外检测、圆二色谱显示元素分布与蛋白结构信号稳定,证明其在体内相关条件下仍保持结构完整(图5f–h)。研究团队进一步将“牙齿纳米盔甲”制备为水性喷雾,使用后可快速在牙面形成盔甲保护层,有望应用于日常口腔护理(图5i–j)。
总结
综上所述,本研究提出了一种完全源自生物质的“牙齿纳米盔甲”,其能够响应口腔中的糖,进而抑制致龋菌活性及生物膜形成,从而实现对龋齿的长效预防。这种“牙齿纳米盔甲”以天然多酚及GOx为构建单元,通过氢键和π–π相互作用等协同作用,在生理条件下自发自组装形成多孔超分子框架。超分子多酚框架的保护作用使GOx在复杂口腔环境中仍能保持持续的催化活性,将葡萄糖不断转化为H2O2,从而显著增强“牙齿纳米盔甲”的抗菌性能。GOx对葡萄糖的持续消耗有效抑制胞外多糖和致龋生物膜的形成,实现长效龋齿预防效果。本研究表明,自组装超分子生物质材料在应对糖诱发的龋病方面具有广阔的应用前景。