缺血性疾病(包括心血管疾病)是全世界造成病人死亡和残疾的主要原因,缺血组织的血管再生是缺血性疾病的主要治疗手段。但是,现有的临床治疗手段(例如注射血管再生相关因子)存在被快速清除和在复杂条件下作用有限的缺点。四川大学制革清洁技术国家工程研究中心郭俊凌教授与香港中文大学Anna Blocki教授联合团队通过硫酸葡聚糖诱导间充质干细胞(MSCs)产生的胶原基细胞外基质(ECM)相互作用,制备了一种有效浓缩了间充质干细胞分泌的促血管生成因子的干细胞胶原纳米颗粒MIPSOS,并将其成功应用于伤口的血管再生。MIPSOS能高效保护MSC细胞分泌蛋白,从而防止其降解和失活,并能对活性成分进行缓释,显著提高了真皮层皮肤损伤的血管重建与伤口愈合(图1)。相关研究成果发表于国际生物医学材料顶级期刊Bioactive Materials,第一作者为德国Saarland University的Thomas Später博士和香港中文大学的Marisa Assunção博士。四川大学制革清洁技术国家工程研究中心博士后龚贵东,副研究员(专职科研)王晓玲参与细胞外基质胶原蛋白自组装及纳米颗粒合成的相关研究。
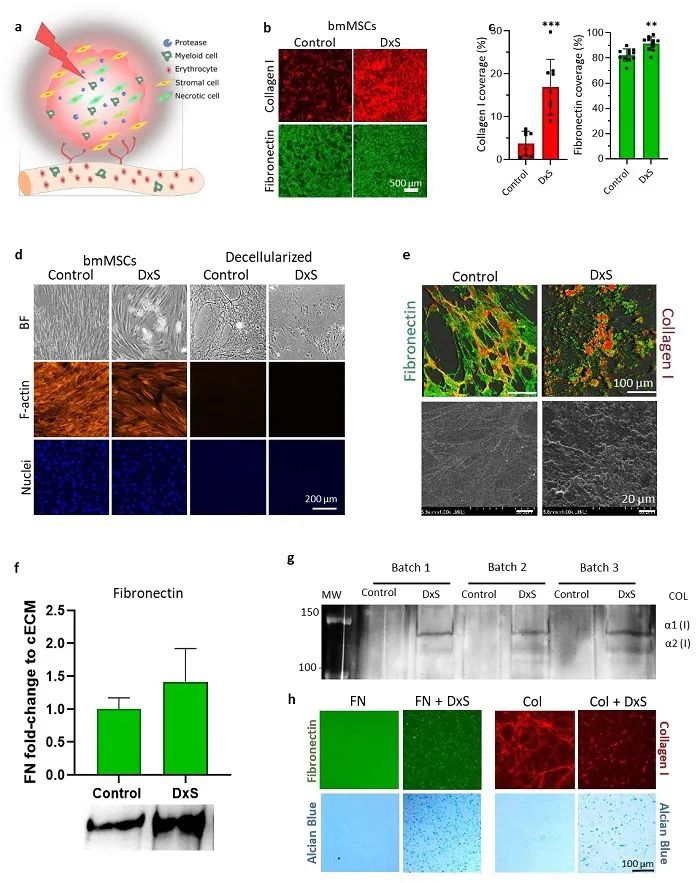
慢性缺血性疾病,如冠状动脉、脑血管和外周血管疾病,是造成全世界死亡和残疾的主要原因。相关组织区域血管生长不足会导致灌注不良,进而导致组织坏死,会进一步阻碍组织再生和伤口愈合。现有的血管重建策略,包括血管生长因子递送和干细胞治疗,尚存在生长因子代谢速度快、剂量不稳定以及移植细胞培养周期长、病灶部位能量供应不足导致细胞死亡等缺点。细胞外基质为血管生长因子的存储与可控释放提供了合适的载体,而MSCs能产生多种细胞因子(包括血管生长因子)。因此,该研究团队将硫酸葡聚糖加入到MSCs培养基中促进细胞外基质和活性细胞因子的分子自组装,其中硫酸葡聚糖刺激MSCs分泌胶原基ECM相关蛋白(如I型胶原和纤连蛋白)(如图2所示),该蛋白进一步组装成为具有生物学活性的纳米颗粒。
图1. 基于间充质干细胞(MSCs)的胶原-生长因子组装纳米颗粒MIPSOS
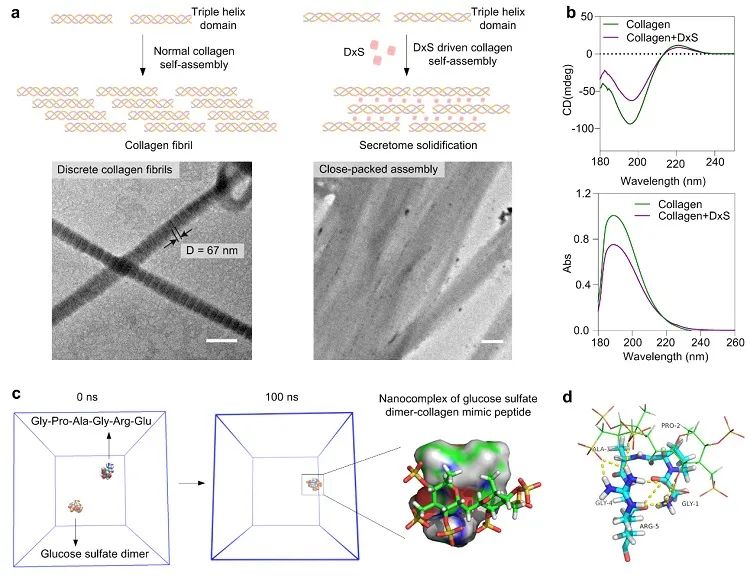
研究团队通过透射电镜、圆二色谱和分子动力学模拟验证了硫酸葡聚糖与细胞外基质(主要成分I型胶原)的相互作用(图2)。结果发现加入硫酸葡聚糖之后,I型胶原中的胶原原纤维堆积更加紧密,同时这种密堆积结构并没有影响胶原的活性。分子动力学计算结果显示硫酸葡聚糖与胶原原纤维之间主要通过范德华力、氢键和静电相互作用结合。
图2. 硫酸葡聚糖与I型胶原之间的纳米结构表征及分子间相互作用
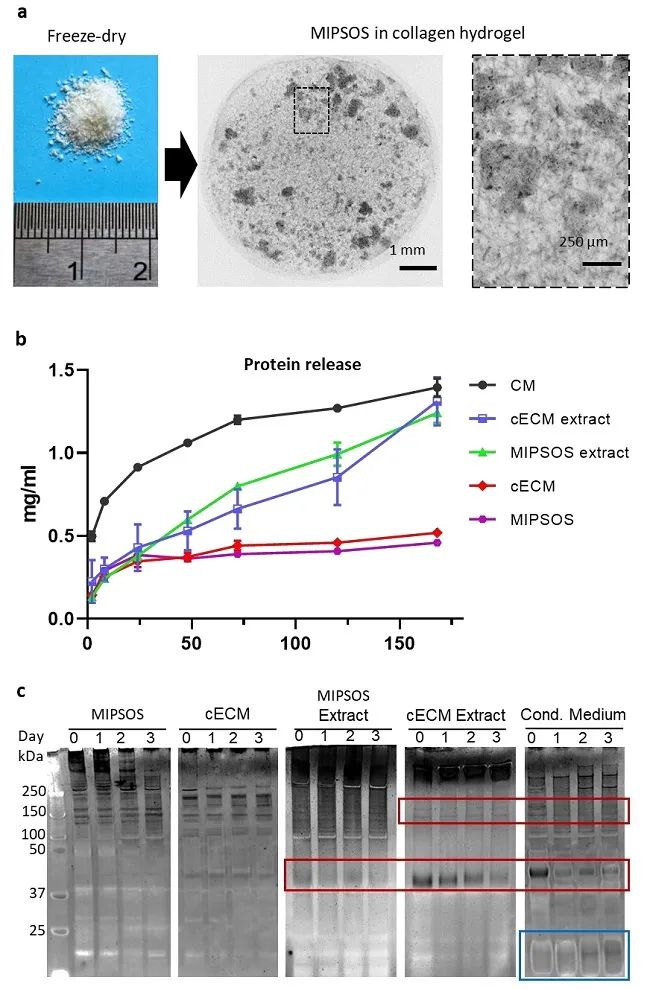
研究团队进一步评价了该体系中活性蛋白质释稳定性(图3)。实验通过检测水凝胶上清液中蛋白质含量,结果发现在cECM和MIPSOS中萃取所得的蛋白质能稳定而迅速地释放。降解实验表明MIPSOS体系能保护包裹于其中的活性蛋白并使其降解速度减慢。
图3. MIPSOS对体系中活性蛋白的保护与控制释放研究
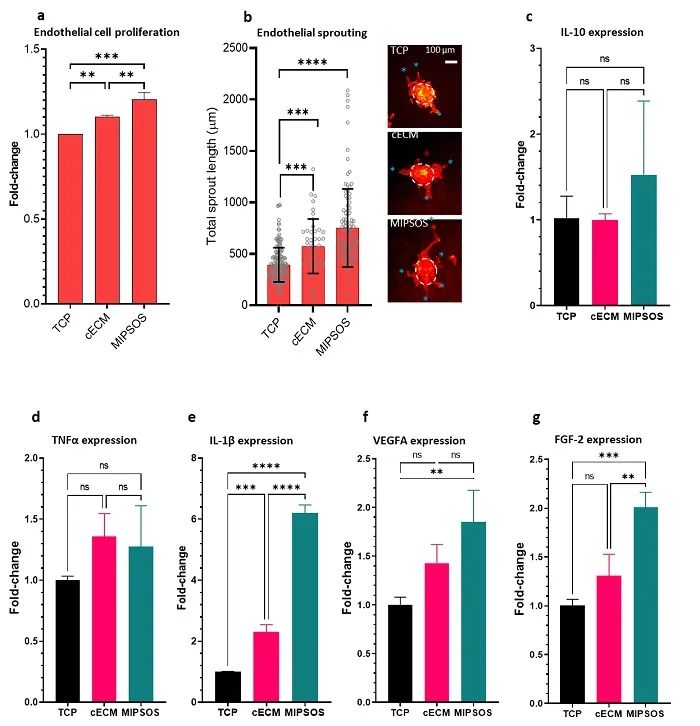
MIPSOS细胞水平的生物活性评价结果发现,MIPSOS能显著增强血管内皮细胞的增值和血管内皮细胞的生长(图4)。使用MIPSOS孵育巨噬细胞后,炎症相关因子(包括IL-10和TNFα)的表达没有显著变化。另外,IL-1β、血管内皮细胞生长因子和FGF-2的表达量都显著升高,说明MIPSOS在诱导伤口血管再生上有明显优势。
图4. MIPSOS细胞水平的活性评价
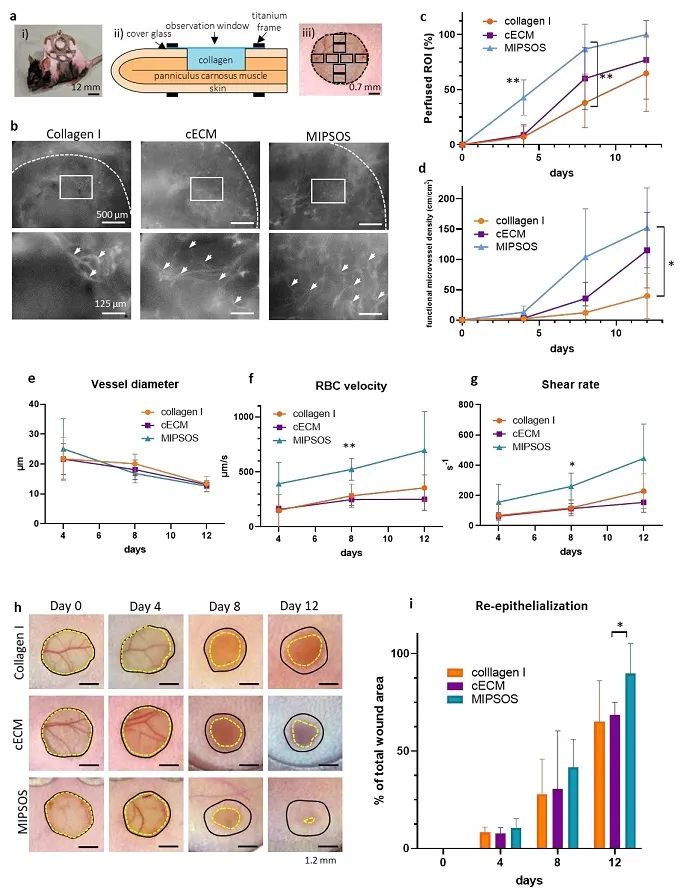
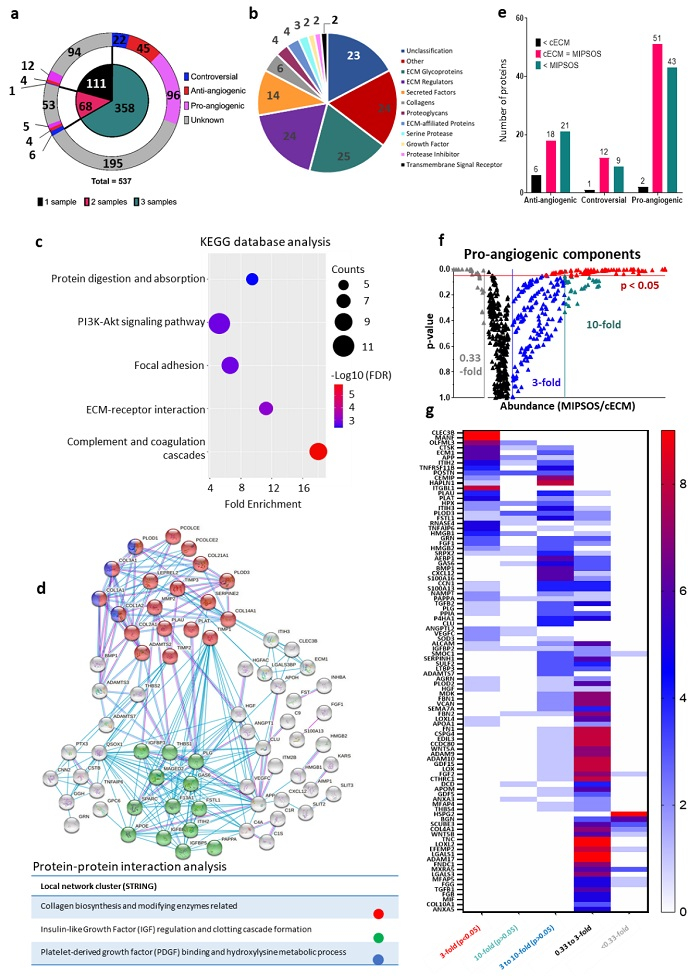
研究MIPSOS的体内活性发现,通过MIPSOS治疗后,小鼠伤口处再生血管数量显著多于对照组(图5)。另外,MIPSOS治疗后伤口愈合速度明显高于对照组。蛋白质组学实验验证了,MIPSOS中细胞因子的含量要远远大于普通ECM中细胞因子含量,这主要是因为MIPSOS具有更好促进伤口愈合的能力(图6)。这种方法将为基于负载细胞源性分泌因子合成具有特定生物活性的新型生物材料开辟新道路,解决干细胞治疗过程中细胞活性难以维持的局限性。同时,该研究结果突出了一种基于颗粒的可存储平台开发,为解决一系列关于血管重建的临床挑战提供更好的促血管生成途径。
图5. MIPSOS促进血管再生的动物实验结果
图6. MIPSOS中的促血管生长因子的分析
原文:
Engineering microparticles based on solidified stem cell secretome with an augmented pro-angiogenic factor portfolio for therapeutic angiogenesis
Thomas Später, Marisa Assunção, Kwok Keung Lit, Guidong Gong, Xiaoling Wang, Yi-Yun Chen, Ying Rao, Yucong Li, Chi Him Kendrick Yiu, Matthias W. Laschke, Michael D. Menger, Dan Wang, Rocky S. Tuan, Kay-Hooi Khoo, Michael Raghunath, Junling Guo, Anna Blocki
Bioact. Mater., 2022, DOI: 10.1016/j.bioactmat.2022.03.015
研究团队介绍
香港中文大学Anna Blocki教授简介
Prof. Blocki Anna joined the Institute for Tissue Engineering and Regenerative Medicine and the School of Biomedical Sciences of The Chinese University of Hong Kong (CUHK) as an Assistant Professor in 2018. She joined the group of Prof. Michael Raghunath within the Department of Bioengineering (now Department of Biomedical Engineering) to pursue her PhD studies on “Peripheral blood: a simple cell source for the generation of angiogenic progenitors from monocytes”. Prof. Blocki was able to secure a PhD scholarship from the Graduate Program in Bioengineering (GPBE) and was later admitted to the top-tier PhD programme, the NUS Graduate School for Integrative Sciences and Engineering (NGS). Her work on Blood Derived Angiogenic Cells (BDACs) allowed her to formulate the hypothesis of more than one origin of pericytes, which she followed up during her later research. Her focus on regenerative cell types and extracellular matrix (ECM) engineering inspired her also to investigate the therapeutic potential of the developed technologies in preclinical studies. This was realized during her first postdoctoral appointment at the Singapore Bioimaging Consortium (SBIC) at the Agency for Science Technology and Research (A*STAR) from December 2012 to April 2015. Following that, Prof. Blocki was able to secure a competitive postdoctoral fellowship from the Charité Universitätsklinikum Berlin that allowed her to work towards ECM-mimicking biomaterials and their potential clinical application.
制革清洁技术国家工程研究中心郭俊凌教授及BMI研究团队

郭俊凌教授,博士生导师,国家高层次人才计划专家、四川省高层次人才计划专家,加拿大英属哥伦比亚大学客座教授,教育部轻工技术与工程学科评估专家,教育部科学技术奖评委专家,成都市“蓉漂计划”国家级领军人才创业项目获得者,成都市高新区产业教授,中国科学技术协会/中国化学会《Chinese Chemical Letters》编委会委员,成都市委统战部“欧美同学会”社会服务专委会副主任,川渝科技学术大会二等奖,四川大学科学技术奖优秀科技人才奖获得者。郭俊凌教授主要参与建立了以植物多酚(植物单宁)和胶原蛋白为核心的生物质基先进材料研究方向,尝试解决包括重大疾病治疗、生殖医学健康、先进农业技术、微生物绿色合成、高效海水提铀、新一代能源电池等多个领域的重要科学问题,受到国内外学者的广泛关注。相关研究以通讯/第一作者在《Science》、《Nature Nanotechnology》、《Nature Communications》、《Science Advances》等国际顶级期刊上发表,共发表论文100余篇,并被多家国际著名新闻媒体报道,包括美国科学促进会EurekAlert!、哈佛Harvard Gazette、德国之音等。依托四川大学国家“双一流”重点建设学科,建立了生物质先进材料研究中心(https://www.bmicenter.org/),带领高度学科交叉的研究团队,开展了以生物质新材料为核心的资源碳中和研究,牵动引领了轻工与跨学科协同发展。